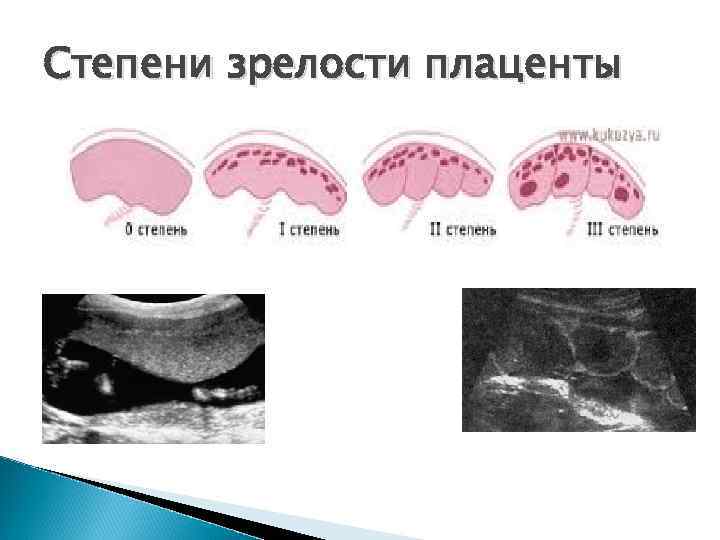
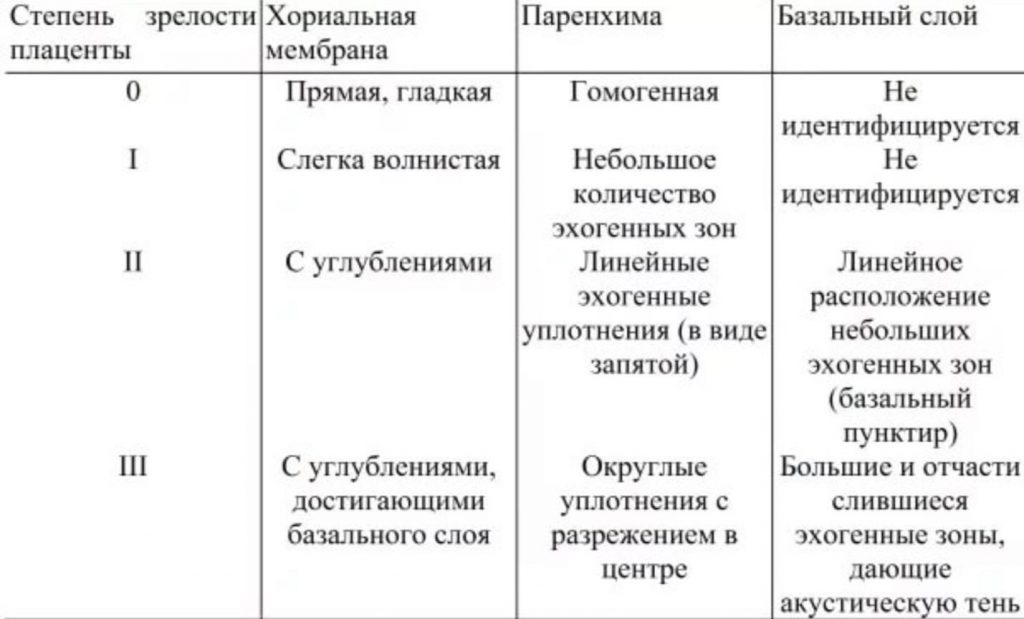
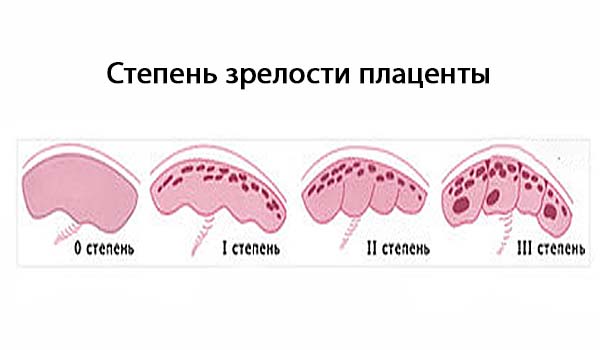
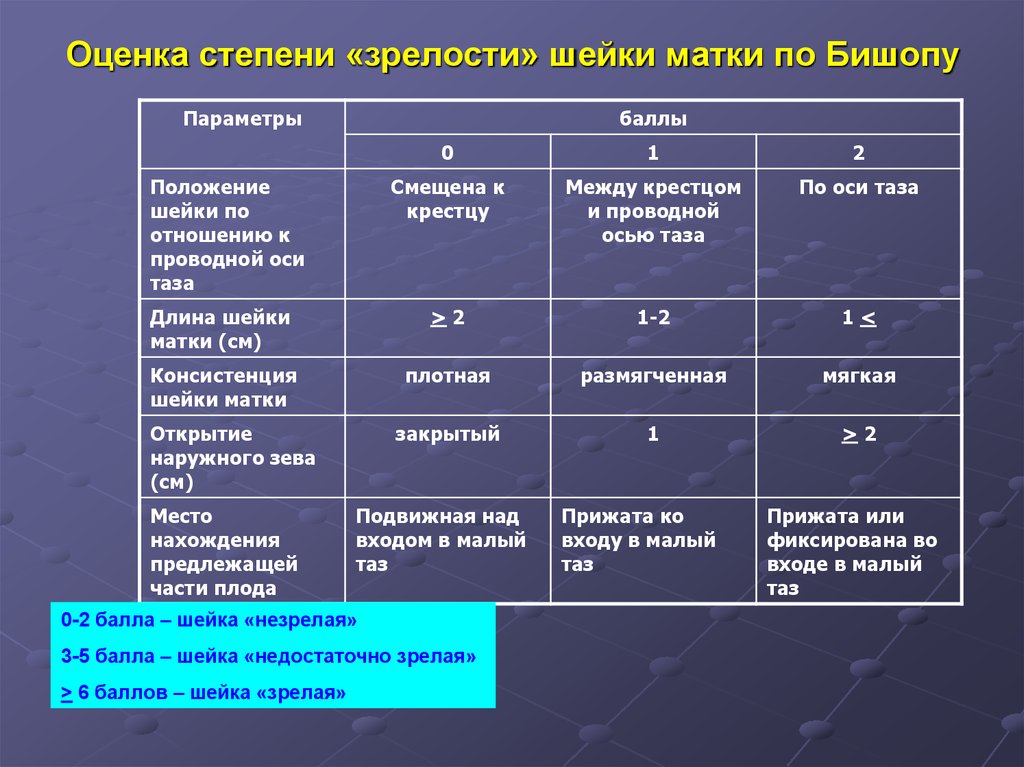
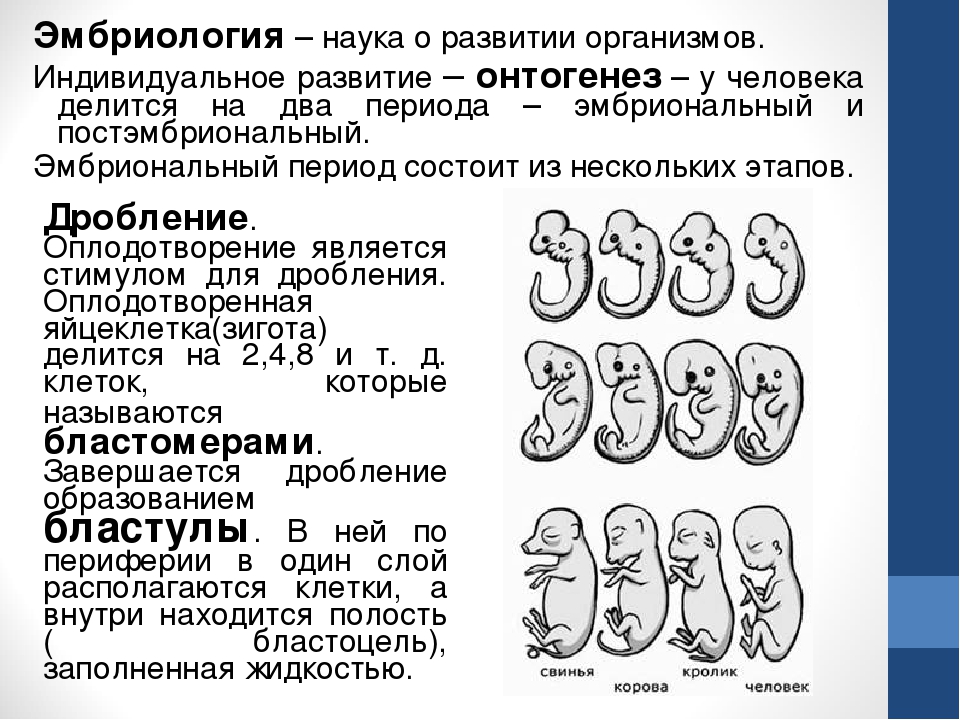
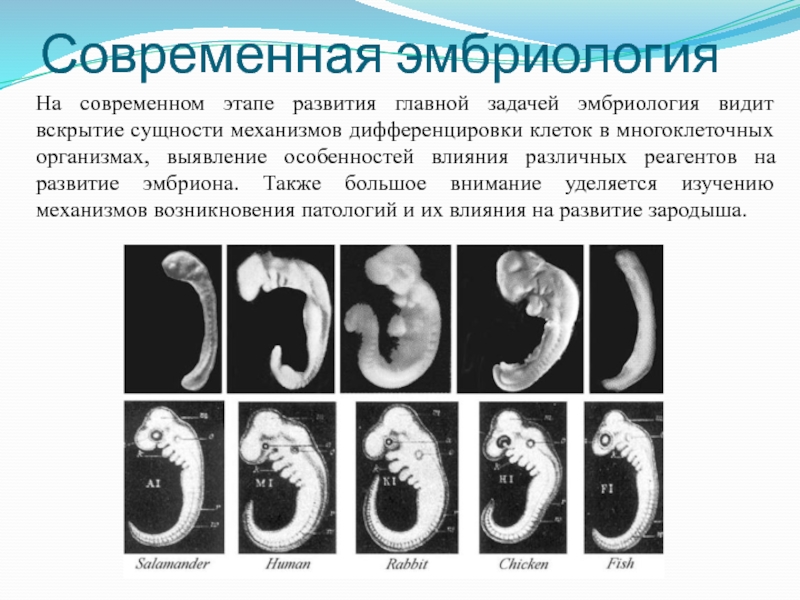
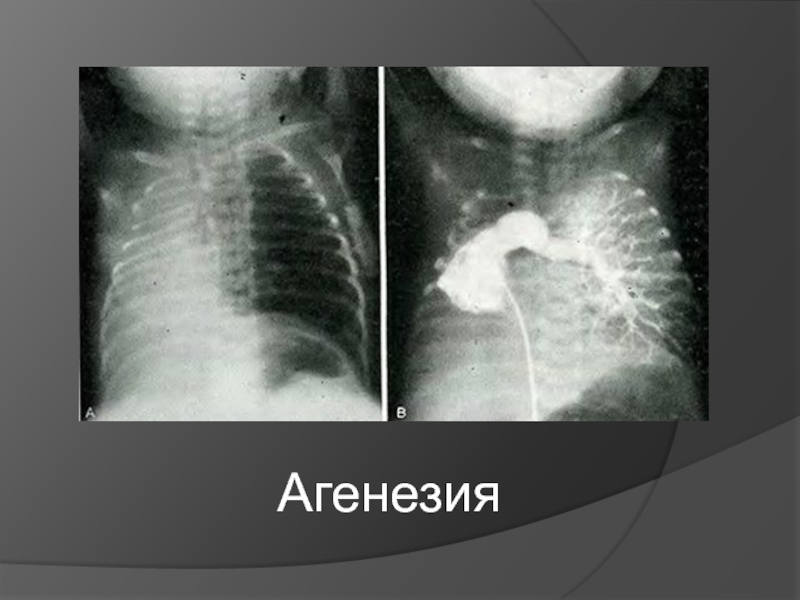
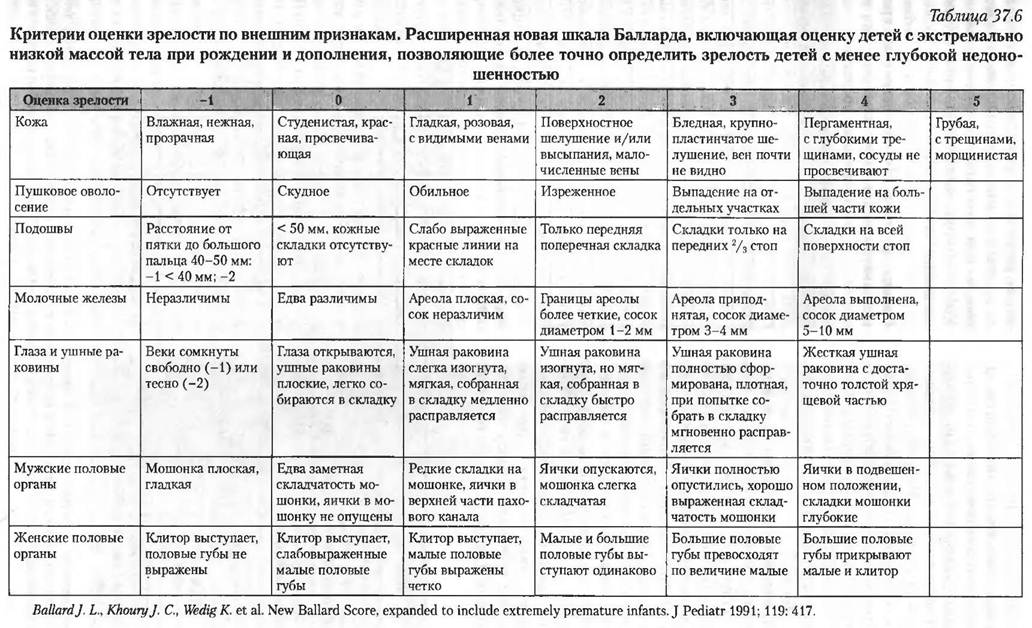
Введение
Зрелость легких плода имеет жизненно важное значение для выживания новорожденных детей и определяет их внеутробную жизни. Респираторный дистресс синдром (РДС) и связанные с ним осложнения вызывают смерть новорожденных в 28% случаев
Однако, широкое пренатальное применение глюкокортикоидов уменьшили заболеваемость РДС. Точная оценка дородовой зрелости легких плода, особенно во время беременности с высокой степенью риска, имеет решающее значение для улучшения неонатального выживания.
Идентификация фосфолипидов в амниотической жидкости, включая фосфатидилглицерол, фосфатидилэтаноламин и соотношение лецитин/сфингомиелин (L/S соотношение), является основным методом определения дородовой зрелости легких, который широко применяется в медицинской практике.
С 1980-х годов многие исследовали использование ультразвука для контроля зрелости легких плода. Исследование эхогенности легких плода, дыхательноподобных движений плода, допплеровского спектра, связанного с назальным потоком жидкости при дыхательноподобных движениях плода (BRNFF) и данные объема легких связаны с анализом зрелости легких плода, однако до сих пор нет единого набора сонографических критериев.
В Китае для ультразвукового исследования развития легких плода нет нормативного диапазона показателей, как определения объема легких, например. Таким образом, данное исследование было проведено (I) для оценки возможности и точности ультразвуковых показателей оценки зрелости легких плода; (II) установления границ нормы объема легких плода и сравнения эхогенности легких к эхогенности печени плода (FLLIR) в китайской популяции.
Врождённые патологии плода — трисомии
Такие патологии встречаются часто, но большинство эмбрионов с хромосомными аномалиями гибнут внутриутробно в результате спонтанных выкидышей. Трисомии имеют генетическую природу и возникают в момент зачатия.
Чтобы предупредить рождение малышей с тяжелыми патологиями, семейным парам, планирующим рождение ребёнка, рекомендуют пройти кариотипирование — изучение хромосомных наборов, позволяющее определить генетическую совместимость и возможность иметь здоровое потомство.
Кариотипирование имеет 99% достоверность, благодаря которой можно заранее узнать, имеют ли супруги предрасположенность к хромосомным мутациям.
На ранних сроках без специальных анализов обнаружить трисомию невозможно. С этой целью проводится перинатальный скрининг — серия анализов, определяющих врождённые аномалии плода. Первый скрининг проводится на сроке 11-13 недель и включает ультразвуковую диагностику и анализы крови на гормоны.
Скрининг проводится добровольно. Но процедуру настоятельно рекомендуется пройти женщинам из группы риска, которые:
- забеременели в возрасте старше 35 лет;
- имели замершие беременности;
- подвергались ионизированному или радиационному облучению;
- работают на предприятиях химической промышленности;
- имеют вредные привычки (курение, употребление алкоголя и наркотиков);
- неблагоприятная экологическая обстановка;
- возраст отца ребенка старше 50 лет.
УЗИ определяет:
- положение эмбриона в матке (исключение внематочной беременности);
- количество плодов (одноплодная или многоплодная беременность);
- форма конечностей, черепа, строение лица;
- сердцебиение;
- устанавливается копчико-теменной размер (высота плода от копчика до темечка);
- нормальное или патологическое строение головного мозга;
- толщина воротникового пространства:
- размер носовой кости:
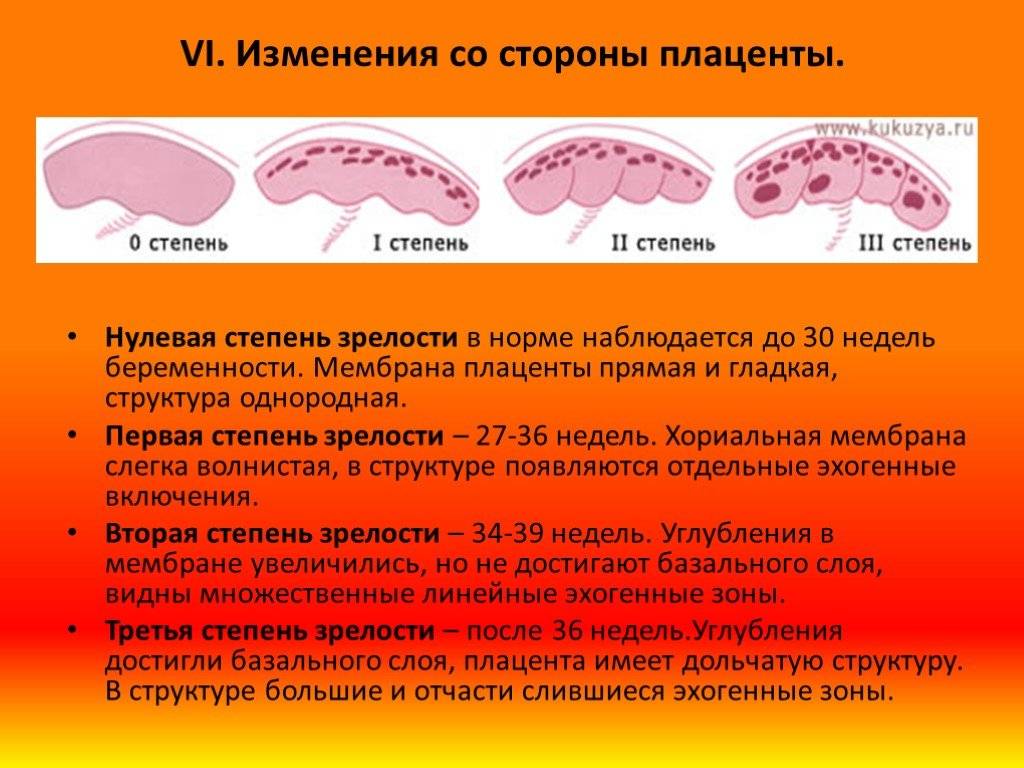
- зрелость и функциональность плаценты.
ОПУХОЛИ ДЕТСКОГО ВОЗРАСТА
Опухоли
у детей значительно более редки, чем у взрослых. Злокачественные
опухоли детского возраста составляют всего 2% всех злокачественных
опухолей. Однако среди причин смерти у детей они стоят на одном из
первых мест. В экономически развитых странах смертность детей от
злокачественных опухолей занимает второе место после несчастных случаев и
составляет 10%.
Опухоли детского возраста имеют следующие особенности.
•
Частое возникновение из эмбриональных тканей в результате
нарушения формирования органов и тканей в период внутриутробного
развития (дизонтогенетические опухоли). Так, 85% злокачественных
опухолей детей до 1 года представлено дизонтогенетическими
опухолями.
• Связь развития опухолей
(онкогенеза) с пороками развития (тератогенезом). У 30% детей с
опухолями различной этиологии диагностируют пороки развития. Опухоль
Вильмса и гепатобластома часто сочетаются с гемигипертрофией, опухоли
ЦНС – с пороками развития мозга, опухоли половых органов – с
пороками половых органов.
• Роль генетических
факторов в развитии опухолей детского возраста. Известно более
100 наследственных синдромов, предрасполагающих к развитию опухолей
у детей. Доказано, что в этиологии ряда врождённых опухолей
генетические факторы играют основную роль. Наследственный характер
установлен для ретинобластомы, нефробластомы, нейробластомы.
•
Доброкачественные опухоли у детей более часты, чем
злокачественные, в отличие от взрослых. Доброкачественные опухоли
составляют более 80% опухолей у детей до 14 лет.
Лечение заболевания
Разработка адекватной тактики лечения пороков развития легких производится пульмонологами и торакальными хирургами. Она основывается на оценке состояния пациента и степени выраженности имеющихся нарушений.
Неотложное хирургическое вмешательство показано в случае выраженной дыхательной недостаточности при наличии аплазии и ангезии легких, лобарной эмфиземы, при трахеопищеводном свище и стенозах трахеи и бронхов.
При кистозной гипоплазии и бронхоэктазах выбор хирургического или консервативного метода лечения определяется количеством измененных сегментов в обоих легких, характером изменений легочной ткани, а также частотой рецидивов.
При распространенных изменениях в легких назначается консервативная терапия, нацеленная на предупреждение обострений гнойного процесса. Она заключается в ежегодных курсах противовоспалительной терапии, улучшении дренажа бронхиального дерева (назначение отхаркивающих и муколитических препаратов, бронхоальвеолярный лаваж, ингаляции, массаж, ЛФК) и санаторно-курортной реабилитации.
Наш сервис сотрудничает с одними из лучших специалистов в области лечения данной патологии. Напишите или позвоните нам для организации консультации у торакального хирурга высшей квалификационной категории, главного торакального хирурга Нижегородской области, зав. хирургическим торакальным отделением ГБУЗ НО «Городская клиническая больница № 5» Фурзикова Д. Л.
Механизм возникновения
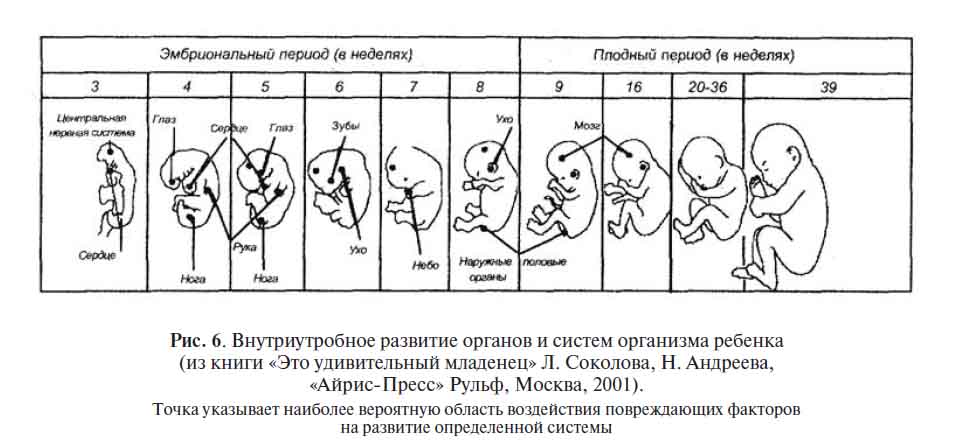
Механизм возникновения пороков развития изучен недостаточно. Считают, что формирование П. р. происходит в результате нарушения процессов размножения, миграции и дифференцировки клеток, гибели отдельных клеточных масс, замедления их рассасывания, нарушения адгезии тканей. Остановка или замедление размножения клеток приводит к аплазии или гипоплазии органа, нарушению слияния отдельных эмбриональных структур, в норме происходящему в строго определенные периоды. В случаях низкой пролиферативной активности клеток контакт между эмбриональными структурами запаздывает. В результате изменений миграции клеток могут развиться гетеротопии, аплазии и ряд сложных пороков. Напр., тяжелые симметричные расщелины лица образуются в результате нарушения миграции клеток нейроэктодермального гребня в верхнечелюстные отростки. Изменение дифференцировки клеток может произойти в любой период эмбриогенеза и быть причиной агенезии органов, их морфол. и функциональной незрелости, а также персистирования эмбриональных структур, напр, неразделения, как это наблюдается при прозэнцефалии. Задержка физиол, распада клеток, отмирающих в процессе эмбриогенеза (напр., при рассасывании межпальцевых перепонок, реканализации кишечной трубки и открытии естественных отверстий), может приводить к синдактилии, атрезии, стенозу. Нарушение адгезивного механизма, т. е. склеивания, удержания и срастания эмбриональных структур, так же как и недостаточно активная пролиферация. является причиной многих дизрафий (напр., П. р., связанных с не-закрытием нервной трубки). В основе формирования нек-рых П. р. лежат циркуляторные расстройства, обусловленные тромбозом, сдавлением, кровоизлиянием. Тератогенный эффект инфекций чаще связан с цитолитическим действием возбудителя.
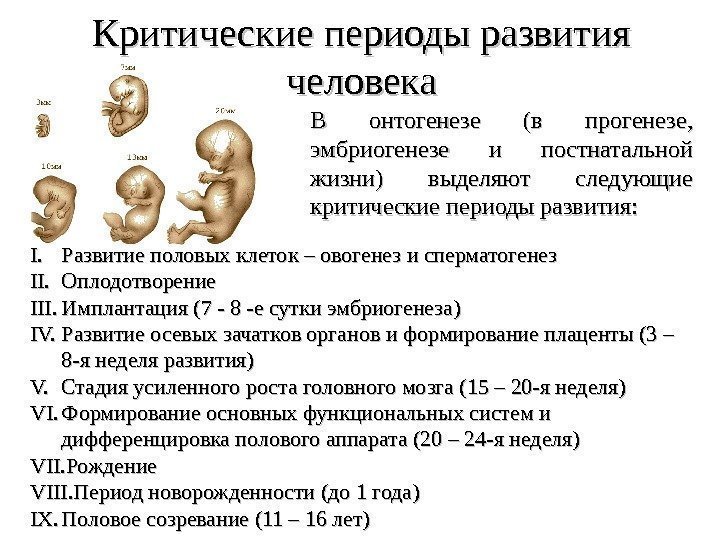
Формирование большинства Пороков развития происходит в течение первых 8—10 нед. беременности. Чувствительность эмбриона к повреждающим факторам в эти сроки различна. По данным П. Г. Светлова, выделяют два отрезка времени повышенной чувствительности, которые называют критическими периодами. Первый из них у человека приходится на конец 1-й — начало 2-й нед. беременности. Действие вредного фактора в это время часто приводит к гибели зародыша. Аналогичное воздействие во второй критический период (3— 6-я нед. беременности) чаще индуцирует П. р. Для установления возможной этиологии П. р. время действия предполагаемого вредного фактора сопоставляют не с критическим, а с тератогенетическим терминационным периодом (ТТП), поскольку каждый П. р. имеет свой ТТП, не всегда совпадающий с критическим периодом. Этот термин, предложенный в 1906 г. Швальбе (Е. Schwalbe), понимается как предельный срок, в течение к-рого действие вредящего фактора может вызвать П. р. Напр., ТТП двухкамерного сердца продолжается до 34-го дня беременности, аплазии межжелудочковой перегородки — до 44-го дня, дефекта межпредсердной перегородки — до 55-го дня беременности. ТТП же для персистирования артериального протока (боталлова протока), крипторхизма, многих П. р. зубов выходит за пределы беременности, т. к. окончательное формирование этих структур не завершается в период внутриутробного развития.
Приобретённые патологии плода
Приобретенные патологии возникают под воздействием негативных факторов (радиация, токсическое отравление) и образа жизни матери (алкоголизм, курение, наркомания).
Врождённые пороки органов и костей
Редко у плода развивается один такой порок, обычно это комплекс патологий, затрагивающих несколько жизненно важных органов.
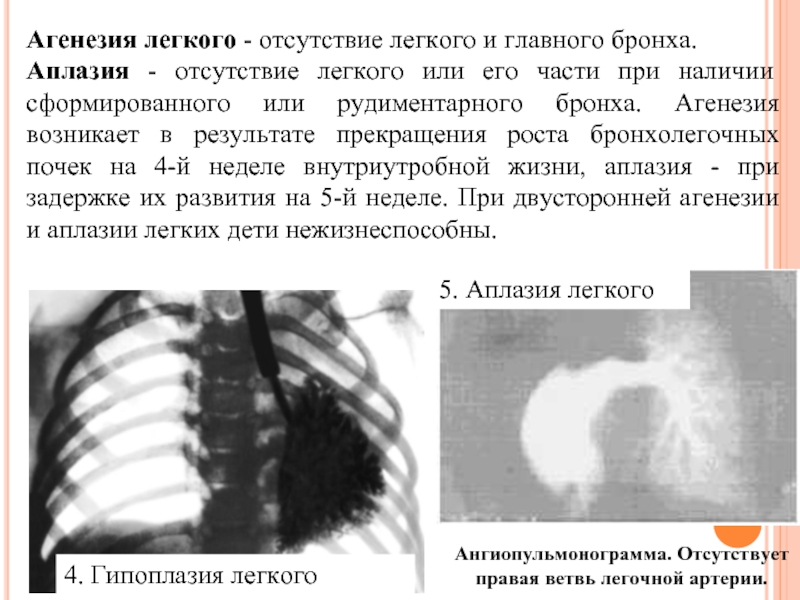
Врождённые пороки имеют следующие разновидности:
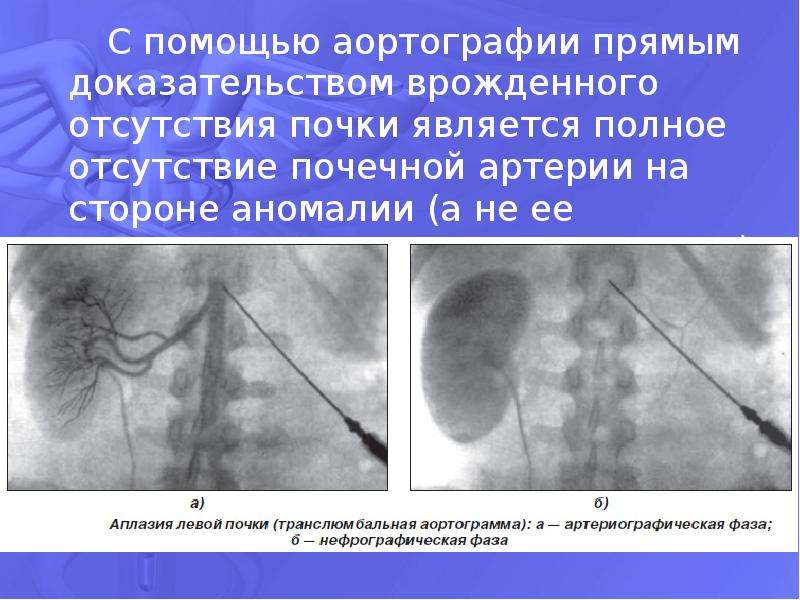
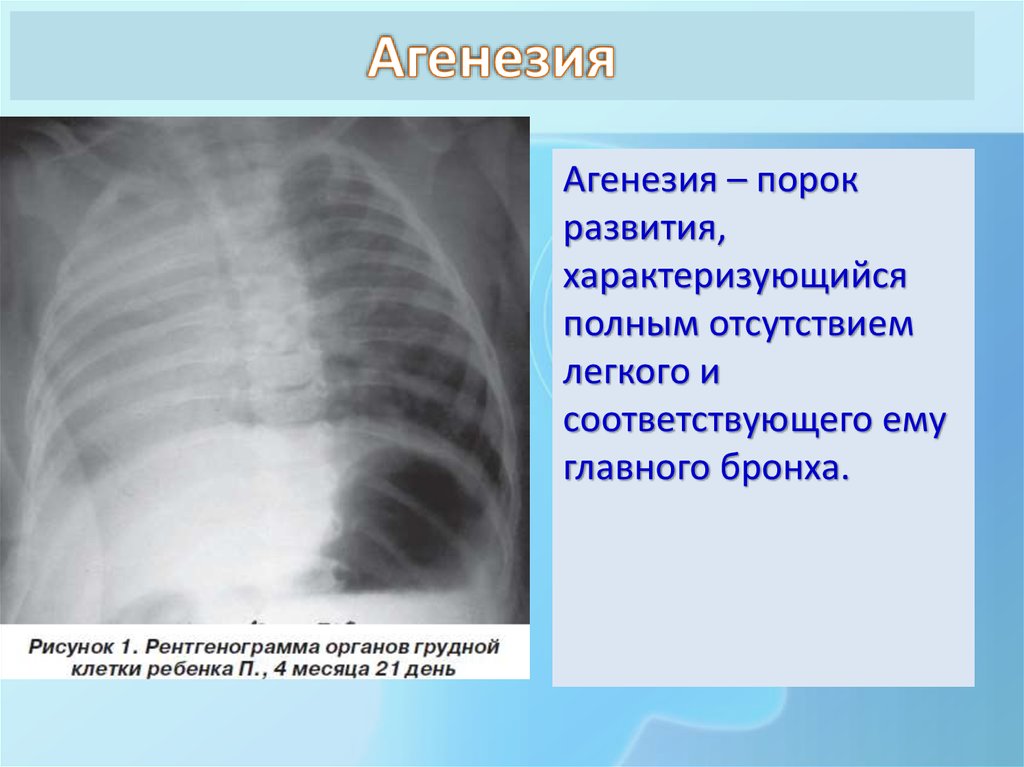
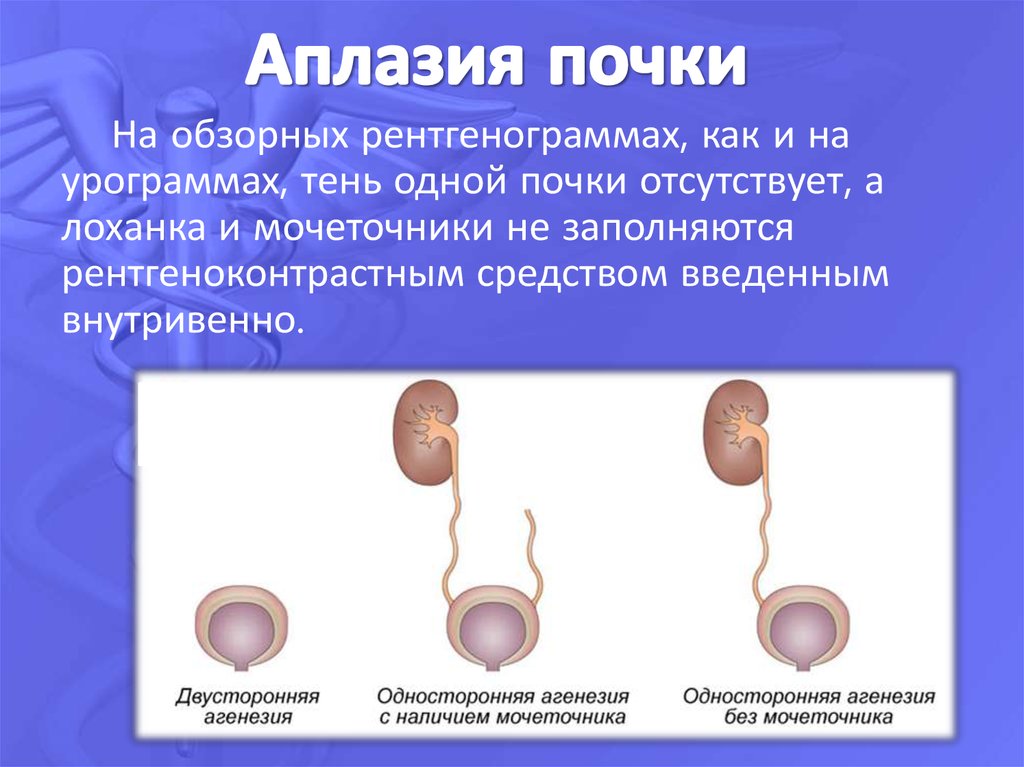
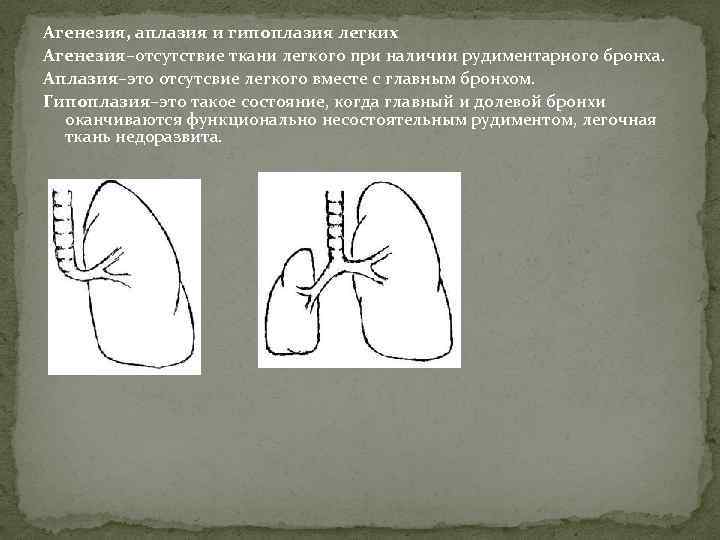
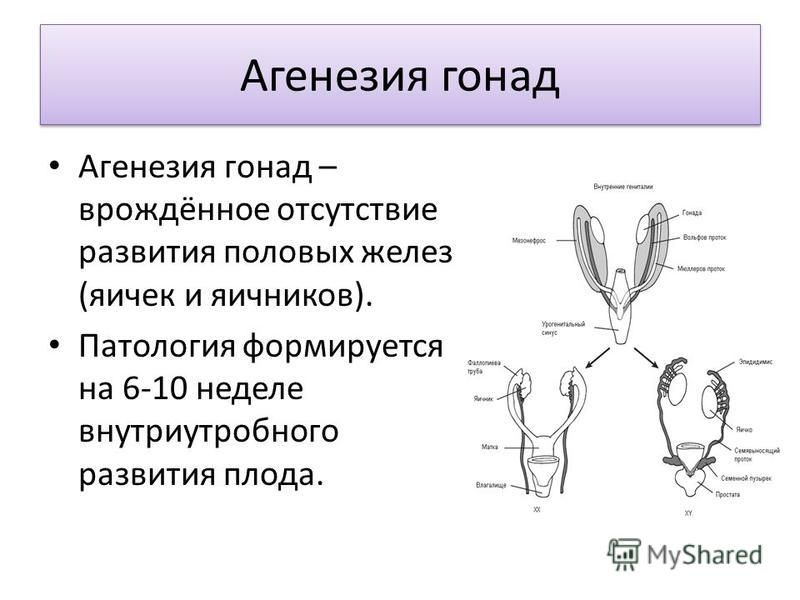
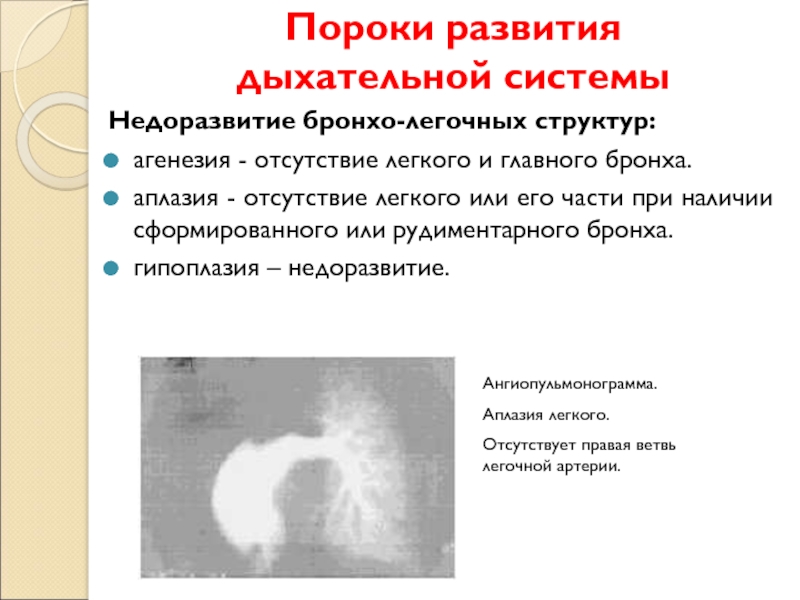
- аплазия — полное отсутствие органа с сохранением сосудистой ножки;
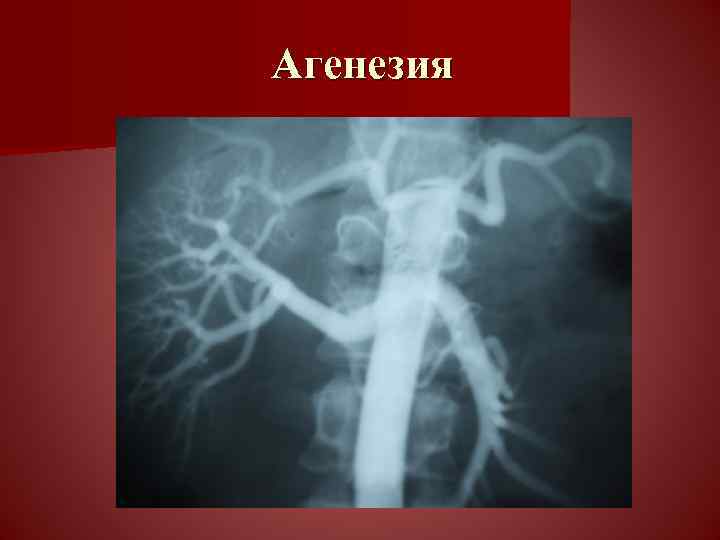
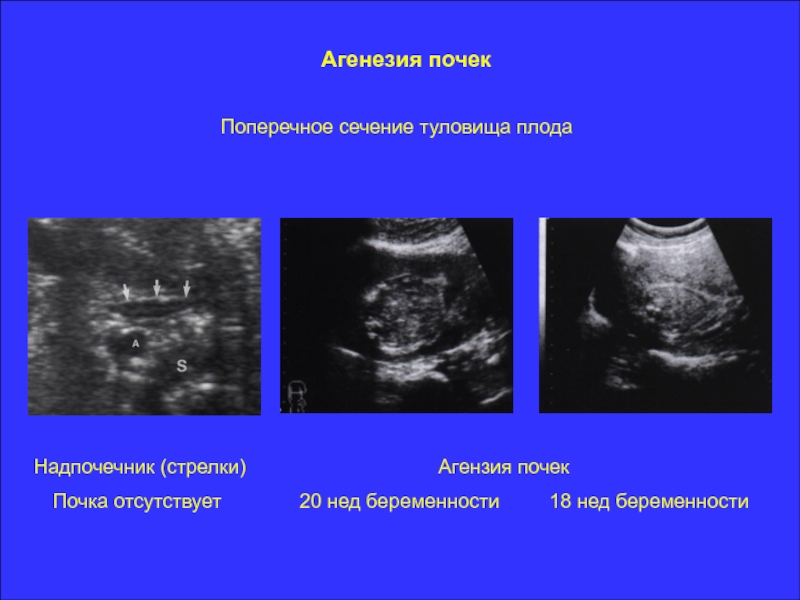
- агенезия — полное отсутствие органа без сохранения сосудистой ножки;
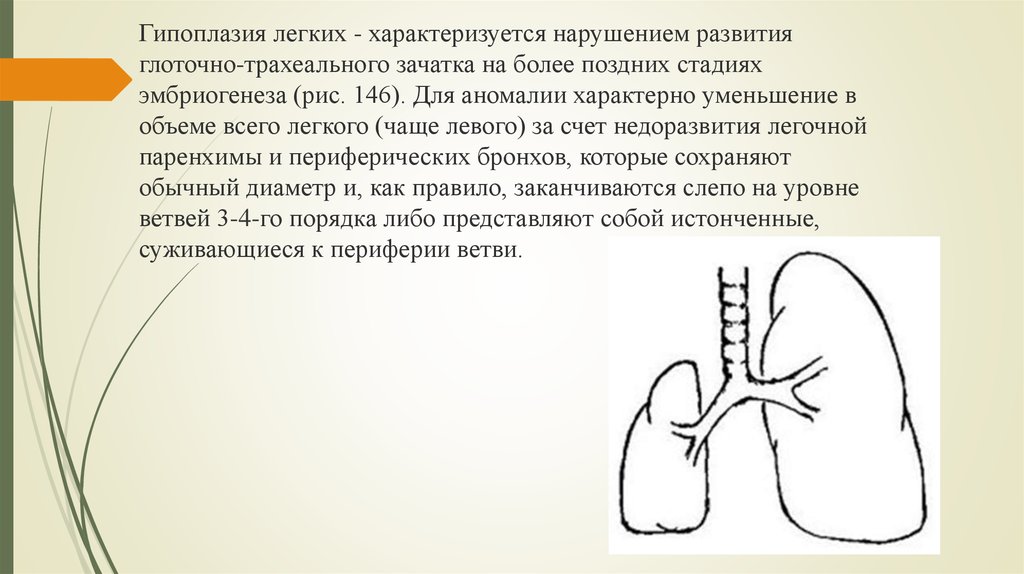
- гипоплазия — недоразвитость органа;
- дистопия — расположение органа в неположенном месте.
Ультразвуковая диагностика врождённых пороков проводится трижды:
- 1-я диагностика — 10-13 недель;
- 2-я диагностика — 19-20 недель;
- 3-я диагностика — 31-32 недели.
Исследование позволяет выявить большинство патологий:
- отсутствие или деформацию органа;
- анэнцефалию (отсутствие головного мозга);
- атрезию (отсутствие) конечностей;
- аномалия скелета лица (заячья губа, волчья пасть);
- незаращение спинномозгового канала;
- пороки сердца;
- гидроцефалия (скопление жидкости в головном мозге).
Гипертензионно-гидроцефальный синдром
Это патология, при которой спинномозговая жидкость скапливается под мозговыми оболочками. Осложнение выявляется на УЗИ на поздних этапах беременности.
Характеризуется большим объёмом головы плода, диспропорцией между мозговыми долями, выпиранием родничка. Чем раньше выявлена патология, тем больше шансов на благоприятный исход.
Гидроцефалия
Это скопление спинномозговой жидкости в желудочках головного мозга, в результате чего они увеличиваются в размерах, и возрастает внутричерепное давление.
Гидроцефалию выявляют на 2 семестре беременности. Главным показателем является увеличение высоты тела желудочка головного мозга выше нормы (свыше 1,1 см). При этом снижается эхогенность межполушарной щели при одновременном увеличении ширины щели свыше 5 мм.
Пороки сердца
Пороки сердца у плода — не редкость. На УЗИ они обнаруживаются на 2-м плановом осмотре (скрининговом УЗИ второго триместра).
К ним относятся:
- гипоплазия левой стороны сердца;
- отсутствие сообщения между правыми камерами сердца;
- отсутствие одного из желудочков сердца;
- патология сердечной мышцы;
- аритмия;
- брадикардия;
- сужение просвета аорты;
- сужение лёгочной артерии;
- порок трикуспидального клапана;
- тетрада Фалло (сочетанная аномалия сердца).
Большая часть сердечных патологий исправляется хирургическим путём. Чем раньше проведена операция, тем больше шансов на успешное выздоровление.
3.Симптомы и диагностика
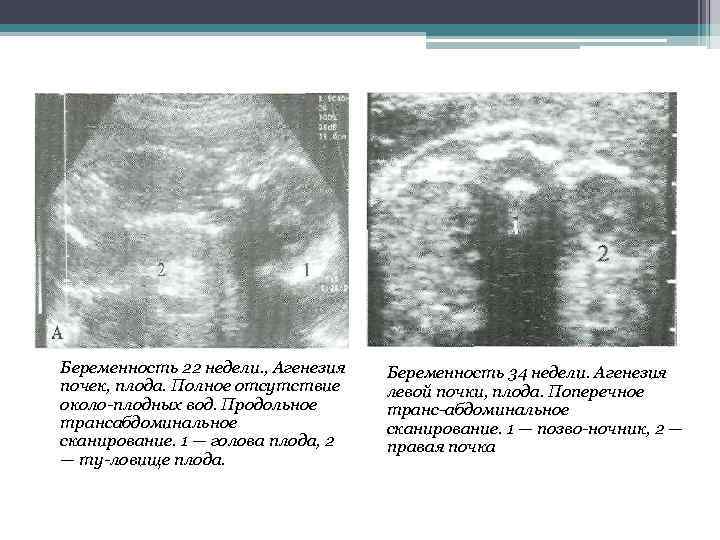
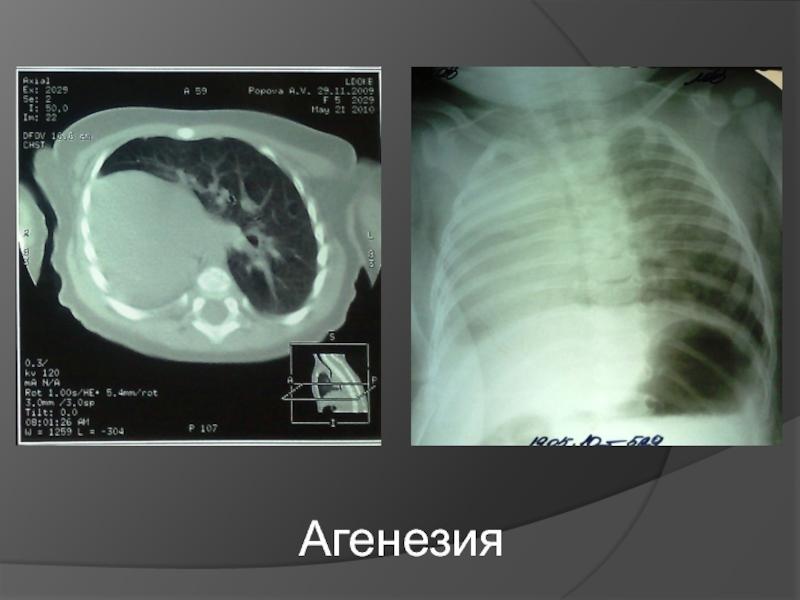
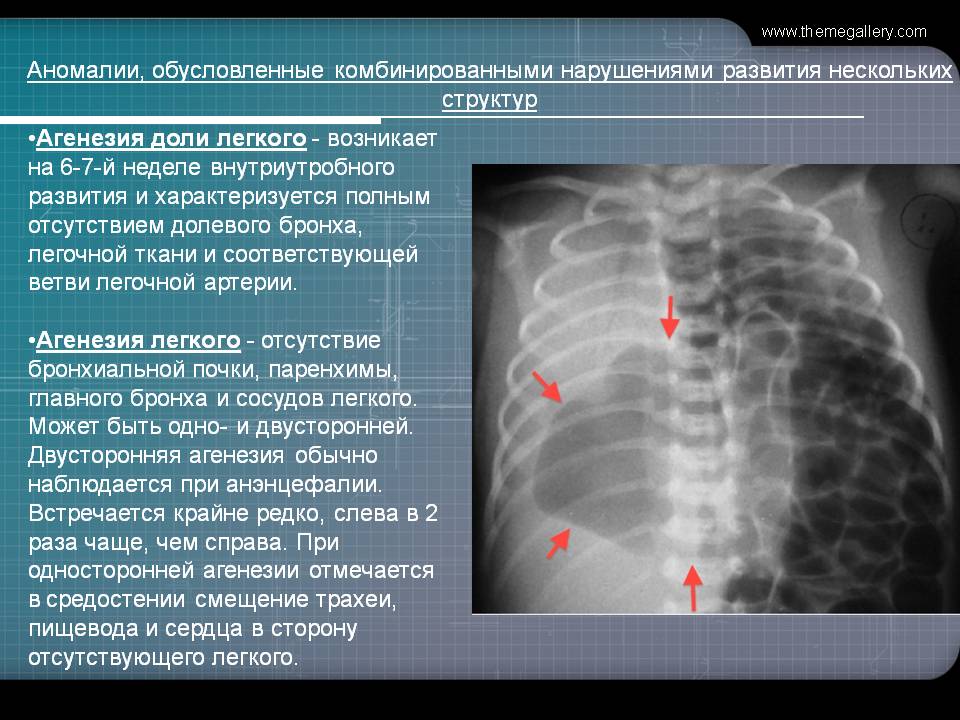
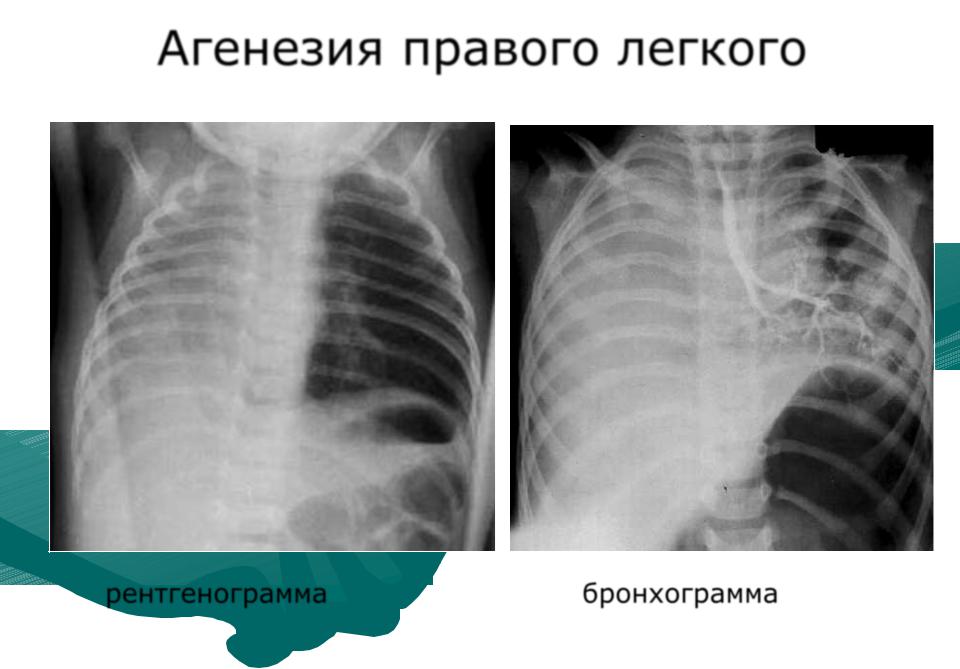
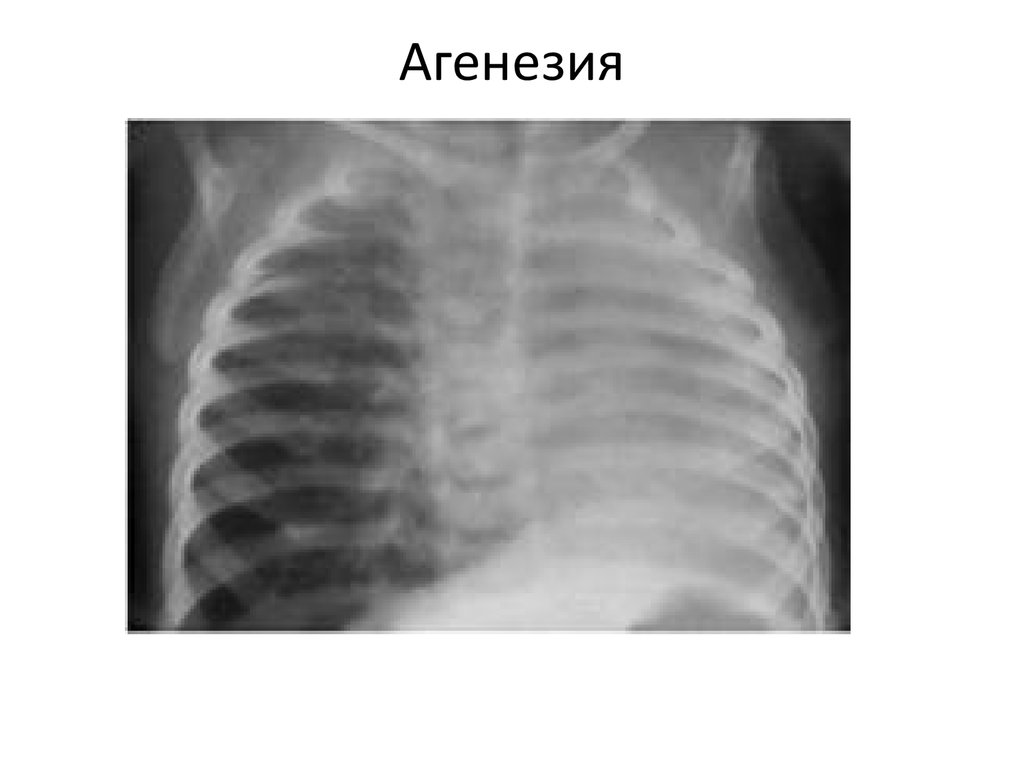
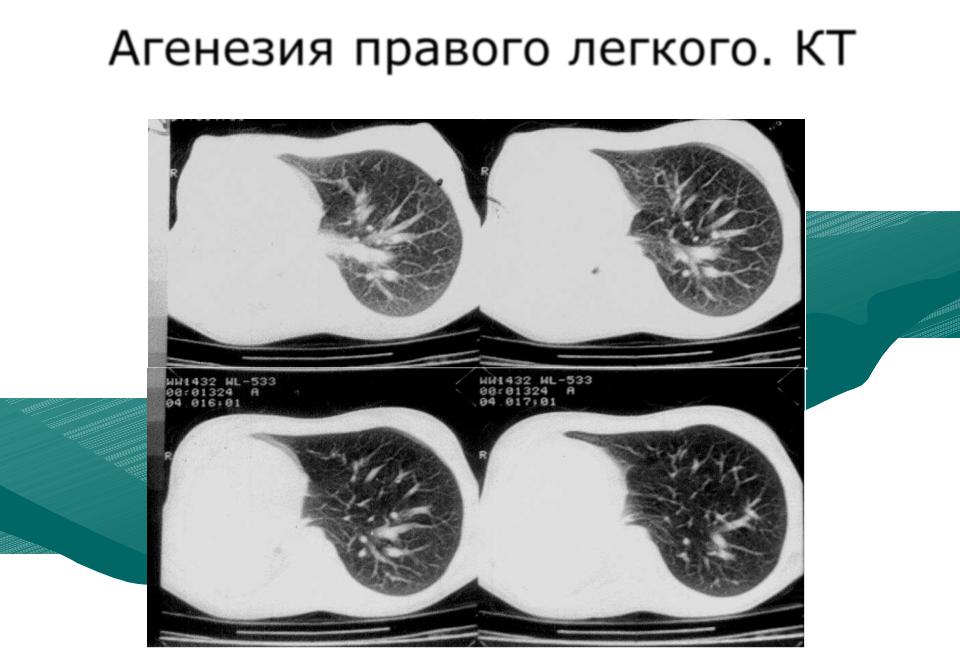
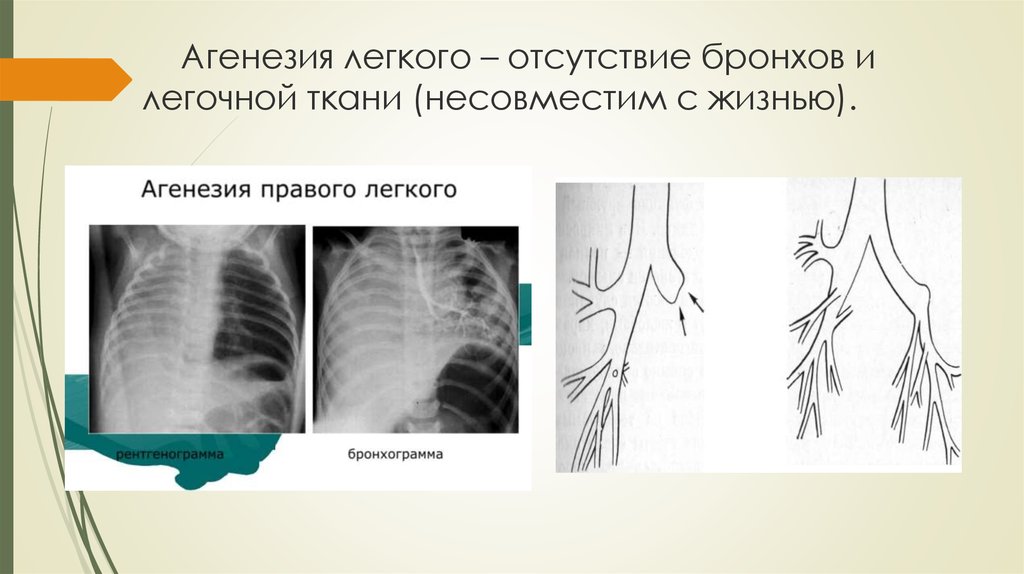
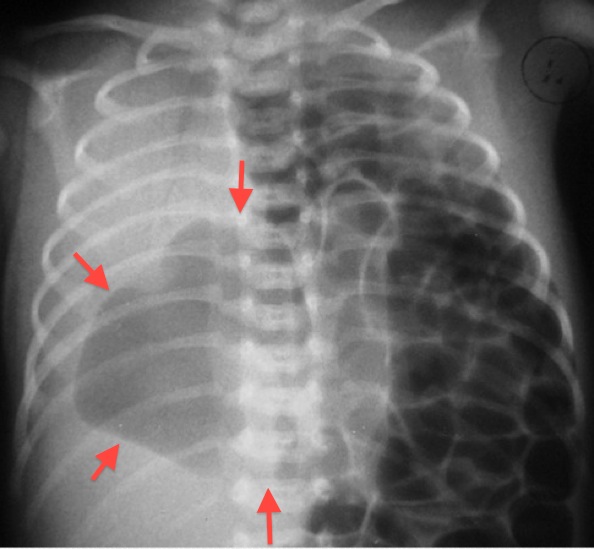
Двусторонняя агенезия несовместима с жизнью.
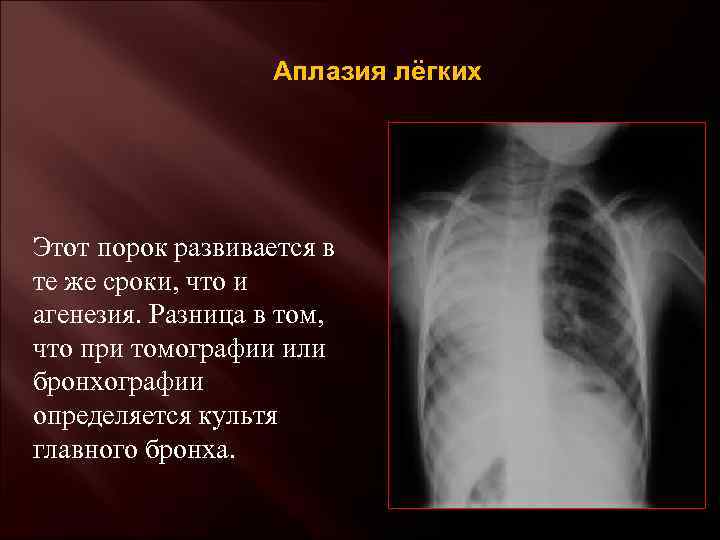
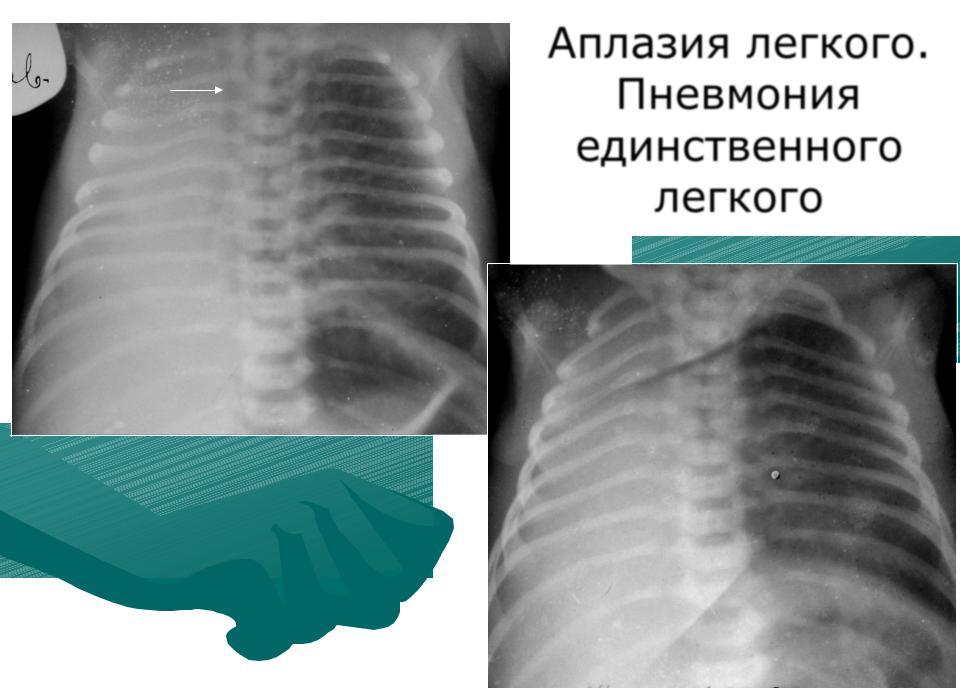
При односторонней чаще отсутствует левое легкое; нередко такая аномалия сочетается с другими пороками внутриутробного развития. Агенезия/аплазия легкого может длительное время протекать мало- или бессимптомно, однако она проявляется асимметрией дыхания при аускультации и притуплением звука при перкуссии. Смещение органов внутри грудной клетки, компенсаторное увеличение сохранного легкого может приводить к ее деформациям. В тяжелых осложненных случаях острая дыхательная недостаточность возникает непосредственно после рождения, быстро нарастает и заканчивается летально.
Гипоплазия клинически делится на две формы, простую и кистозную (врожденный поликистоз), при которой, как правило, имеет место хронический воспалительный процесс в дыхательной системе (с соответствующей симптоматикой).
Следует понимать, что столь серьезные аномалии, как агенезия, аплазия или гипоплазия легкого не может не сказываться на эффективности дыхания и газообменных процессов. В той или иной степени (от субклинической до критически тяжелой) дыхательная недостаточность присутствует во всех случаях; наличие порока отражается на качестве жизни, внося существенные ограничения, и является одним из факторов сокращения ее продолжительности.
Агенезия и гипоплазия легкого может быть предположительно диагностирована уже при стандартном осмотре и аускультации. Такие пороки развития легко подтверждаются рентгенологически. Как правило, назначается также ангиопульмонография.
Патологии плода, вызванные алкогольной зависимостью беременной
Самая распространённая патология, вызванная употреблением алкоголя беременной женщиной, — синдром Миллера-Дикера. Мутация происходит в гене 17-й хромосомы. Главная причина аномалии — интоксикация плода альдегидами, передающимися через материнскую кровь.
На УЗИ синдром Миллера-Дикера выражается в многоводии, отставании внутриутробного развития плода и снижении его двигательной активности. На более поздних сроках можно увидеть утолщение коры головного мозга при разглаживании мозговых извилин.
Голова у больных детей меньше положенного размера, лоб выпуклый, плоский затылок, челюсть недоразвита (алкогольная дизморфия). Ушные раковины расположены ниже положенного уровня, пальцы неправильной формы, тазобедренные суставы находятся на зачаточном уровне, стопы укорочены, задний проход сросшийся.
Такие дети обычно умирают в возрасте в 2 лет из-за аспирационной пневмонии. У них глубокая умственная отсталость и отсутствуют даже обычные рефлексы (глотание, моргание).
ПАТОЛОГИЯ ПЕРИНАТАЛЬНОГО ПЕРИОДА
Перинатальный
период – период с 22-й полной недели (154-го дня) внутриутробной
жизни плода до семи полных суток после рождения ребёнка.
Неонатальный период начинается с момента рождения и заканчивается через 28 дней жизни ребёнка.
Живорождение –
полное изгнание или извлечение продукта зачатия из организма матери
независимо от продолжительности беременности, если плод имеет при
рождении любой из четырёх признаков жизни: самостоятельное дыхание,
сердцебиение, пульсацию сосудов пуповины, произвольные движения
мускулатуры.
Мертворождение – смерть продукта
зачатия, наступившая до его полного изгнания или извлечения из организма
матери. Смерть, наступившая до начала родовой деятельности, называют
антенатальной, смерть во время родов – интранатальной. Смерть
плода, наступившую ранее 28 нед беременности, делят на раннюю (до
20 нед) и позднюю (21-28 нед).
Младенческая смертность – число детей, умерших в возрасте до 1 года на 1000 живорождённых.
Неонатальная
смертность – число детей, умерших в возрасте до 28 суток на
1000 живорождённых. Выделяют следующие виды:
∨ ранняя неонатальная смертность – смертность новорождённых в течение первых 7 сут жизни;
∨ поздняя неонатальная смертность – смертность новорождённых с 8-го по 28-й полный день жизни.
Перинатальная
смертность – число рождённых мёртвыми и умерших в первые
6 сут после рождения на 1000 рождённых живыми и мёртвыми.
Показатели перинатальной смертности значительно неодинаковы в разных
странах – от 12 до 50‰. В России этот показатель в 1999 г
составил 14,3‰.
Симптомы
Клинические проявления недоразвития легких зависит от выраженности гипоплазии одного или обоих легких, наличия инфекционных осложнений. Гипоплазия 1 и 2 сегментов легких может отличатся бессимптомным течением. Недоразвитие одной и более долей обусловлено появлением симптомов различной степени выраженности. Симптоматика простой и кистозной гипоплазии мало чем отличается.
В большинстве случаев малыши с гипоплазией легких, отстают в физическом развитии. У них может выявляться деформация грудной клетки и искривление позвоночника в сторону здорового легкого. Больные могут жаловаться на появление болей в грудной клетке и кровохарканья. При прогрессирующей форме дыхательной недостаточности у пациентов отмечается развитие одышки во время физических нагрузок, акроцианоза, а с течением времени формируется деформация ногтевых фаланг. При присоединении вторичной инфекции развивается симптоматика типичная для хронической пневмонии. При частых, практически непрерывно рецидивирующих обострениях отмечается возникновение субфебрилитета, влажного кашля, слизисто-гнойной или гнойной мокроты и стойкого недомогания.
Течение гипоплазии легочной ткани может отягощается наличием у больного множественных аномалий развития. Иногда гипоплазия и аплазия легких сочетаются с врожденными пороками сердца, пищеварительной и костно-мышечной систем. Довольно часто легочные аномалии входят в структуру врожденных синдромов. При продолжительном течении патологии и отсутствии ее хирургической коррекции, может возникать легочная гипертензия, легочное сердце, пневмоторакс, хронический бронхит, вторичные бронхоэктазы, а в редких случаях амилоидоз.
Причины множественных врожденных пороков развития
Все этиологические факторы МВПР можно разделить на две группы:
- эндогенные — включают в себя генные, геномные и хромосомные мутации, заболевания эндокринной системы, метаболические нарушения, возраст родителей;
- экзогенные — физические (травмы), химические (лекарственные препараты, промышленная и бытовая химия) и биологические (вирусы, бактерии) агенты.
Эти причины приводят к хромосомным, генным и геномным нарушениям, влияют на процессы клеточного и тканевого развития. Большое число множественных врожденных пороков (МВПР) отличаются типом наследования, патогенезом, клиническими проявлениями, прогнозом для пациента.
Лечение
Консервативное лечение гипоплазии легких малоэффективно и позволяет только временно ограничить прогрессирование вторичных изменений в легких и бронхах. Веским поводом для отказа от проведения хирургического лечения является двустороннее поражение с 10 по 12 сегмент, тяжелая сердечно-легочная недостаточность, легочная гипертензия, хронические декомпенсированные заболевания и наличие у пациента новообразований.
Наличие у больного хронического инфекционно-воспалительного процесса в гипоплазированном легком – это прямое показание к оперативному вмешательству, обусловленное удалением патологического участка или всего легкого.
ГНОЙНО-СЕПТИЧЕСКИЕ ЗАБОЛЕВАНИЯ НОВОРОЖДЕННЫХ
Анатомо-физиологические
особенности, сниженная иммунная реактивность обусловливают высокую
восприимчивость новорожденных к гнойно-воспалительным инфекциям.
Инфицирование может наступить как во внутриутробном периоде, так и сразу
после рождения.
У новорожденных грань между
локальными и генерализованными формами гнойной инфекции в значительной
мере условна, так как возможен быстрый переход местного воспалительного
процесса в генерализованную инфекцию.
Клокальным формам относятся гнойно-воспалительные заболевания кожи и слизистых оболочек.
Кожа
новорожденных подвергается инфицированию наиболее часто. Различные
клинические формы поражения при этом объединяют под названием пиодермии.
Пиодермии развиваются под воздействием гноеродных микроорганизмов
(стафилококки, стрептококки, гонококки, протей, кишечная палочка,
синегнойная палочка и др.).
Везикулопустулез – поверхностная
стафилодермия новорожденных – встречается наиболее часто. Процесс
локализуется в устьях экзокринных потовых желез. Возникновению
заболевания могут способствовать перегревание, повышенная потливость,
мацерация. Фолликулярные пустулы размером с просяное зерно или горошину
располагаются по всему кожному покрову, чаще локализуются на спине, в
складках, на коже шеи, груди, в области ягодиц и на волосистой части
головы. Лечение местное (бриллиантовая зелень, метилвиолет, 2% раствор
перманганата калия). Антибактериальная терапия, как правило, не
проводится.
Псевдофурункулез – заболевание
мерокринных потовых желез у детей грудного возраста (множественные
абсцессы потовых желез, псевдофурункулез Фингера). Развитию заболевания
способствуют недоношенность, иммунодефицитные состояния, искусственное
вскармливание, дефекты ухода, повышенная потливость. Высыпания чаще
всего располагаются на затылке, спине, ягодицах, бедрах, возможно
распространение на кожу груди и живота. Заболевание сопровождается
нарушением общего состояния с повышением температуры тела. Местное
лечение осуществляют 2% спиртовыми или водными растворами анилиновых
красителей, присыпками из окиси цинка (10 %) с тальком. По показаниям
назначают антибиотики (с учетом данных антибиотикограммы) и
иммунозаместительную терапию.
РОДОВЫЕ ТРАВМЫ
Под
родовой травмой подразумевают механическое повреждение плода (нарушение
целостности тканей и органов), возникающее при прохождении через
родовые пути. Различают родовые повреждения центральной и периферической
нервной системы, мягких тканей и костей плода. Внутричерепные
кровоизлияния могут также возникать на фоне хронической и острой
гипоксии, особенно у недоношенных детей.
Причиной
родовой травмы у новорожденного могут быть быстрые, стремительные и
затяжные роды, крупная масса плода, сужение размеров таза, влагалищные
родоразрешающие операции (наложение щипцов, вакуум-экстракция, поворот
плода и извлечение его за ножку) при отсутствии необходимых условий или
нарушении техники.
Хроническая и острая гипоксия плода повышают вероятность родовой травмы.
Повреждения ЦНС (головного и спинного мозга). Травматические повреждения головного мозга
(кровоизлияния) возникают относительно редко, чаще их причиной является
гипоксия. Различают эпидуральные, субдуральные, субарахноидальные и
внутримозговые кровоизлияния, которые нередко сопровождаются
повреждением костей черепа, твердой мозговой оболочки и ее производных
(венозные синусы, намет мозжечка и др.). Эпидуральные кровоизлияния
локализуются на внутренней поверхности черепа между костью и
надкостницей, субдуральные кровоизлияния – между твердой и мягкой
мозговыми оболочками, субарахноидальные кровоизлияния – между паутинной
оболочкой и поверхностью полушарий головного мозга.
Вне
зависимости от генеза клиническая картина у новорожденных зависит от
локализации и размеров кровоизлияния, а также от сопутствующих
повреждений.